1. Aluminium
a.sifat fisis
Aluminium merupakan logam yang
lunak, ringan dengan dengan kenampakan seperti perak yang di sebabkan oleh
lapisan tipis hasil oksidasi (Al2O3). Aluminium merupakan
logam yang tidak beracun (nontosik), tidak memiliki sifat magnetik dan tidak
mengeluarkan percikan api. Aluminium memiliki kekuatan tarik sekitar 49
megapascal (MPA) dalam keadaan murni dan 400 Mpa sebagai paduan sebagai paduan
(alloy), dapat ditempa dan mudah dicetak. Aluminium juga sebagai konduktor yang
baik.
b.Sifat kimia
-reaksi thermit
Fe2O3(s) + 2Al(s)
Al2O3(s) + 2Fe (l)
Aluminium apabila bereaksi dengan
asam menghasilkan H2
2Al(s) + 6H+(aq)
2Al 3+(aq) + 3H2(g)
Aluminium juga dapat bereaksi dalam
suasana basa
2Al(s) + 2OH-(aq)+6H2O 2[Al(OH)4]- (aq) + 3H2(g)
c.Mineral Aluminium
terdapat dalam bentuk
senyawa aluminosilikat (Al2Si2O5)(OH)4, yaitu suatu mineral yang mengandung
aluminium, silikon dan oksigen.
mineral yang merupakan sumber aluminium
hanyalah bauksit (Al2O3nH2O). Mineral lainnya yang cukup bernilai yaitu kriolit
(Na3AlF6) dan veldspath/spat padang (KAlSi3O8).
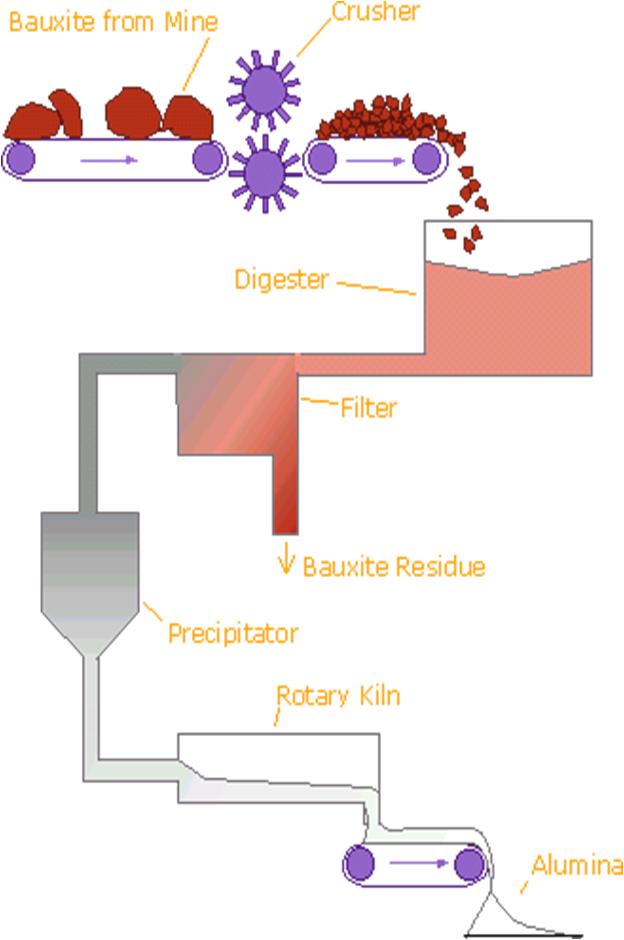
d.Proses Pembuatan Aluminium
Cara penambangan bauksit dengan cara dihaluskan , dicuci dan
dikeringkan, sesudah itu bauksit mengalami pemurnian menjadi oksida aluminum
atau alumina. Bauksit halus yang kering dimasukkan ke dalam pencampuran, diolah
dengan soda api (NaOH) di bawah pengaruh tekanan dan pada suhu di atas titik
didih.
e.Kegunaan Aluminium dan Senyawanya
Thermit (campuran A1 dan Fe2O3)
digunanakan untuk mengelas logam,
Aluminium sulfat (A12(SO4)3.
17H2O) digunakan pada pewarnaan tekstil,
K2SO4(SO4)3.
24H2O KAI(SO4)2. 12H2O yang dikenal
dengan tawas digunakan untuk menjernihkan air,
Sebagai bahan pembersih bersama
dengan padatan N3OH. Jika keduanya ditambahkan air, akan dihasilkan
panas yang dapat membantu melelehkan lemak dan minyak pernyumbat dan kemudian
dapat terlarut dalam NaOH(aq),
Bubuk aluminium digunakan untuk
menjalankan roket, dan
Digunakan pada industri otomotif,
yaitu untuk badan mobil dan velg.
2.Timah
a.Sifat Fisis
Simbol : Sn
Radius Atom : 1.62
Å
Volume Atom : 16.3
cm3/mol
Massa Atom : 118.71
Titik Didih : 2876 K
Radius Kovalensi : 1.41
Å
Struktur Kristal : tetragonal
Massa Jenis : 7.31 g/cm3
Konduktivitas Listrik : 8.7 x 106 ohm-1cm-1
Elektronegativitas : 1.96
Konfigurasi Elektron : [Kr]4d10 5s2p3
Formasi Entalpi
: 7.2 kJ/mol
Konduktivitas Panas : 66.6 Wm-1K-1
Potensial Ionisasi : 7.344 V
Titik Lebur : 505.12 K
Bilangan Oksidasi : 4,2
Kapasitas Panas
: 0.228 Jg-1K-1
Entalpi Penguapan : 290.37 kJ/mol
b.Sifat Kimia
larutan yang mengandung ion
timah(II) (misalnya larutan timah(II) klorida) akan mereduksi larutan iod
menjadi ion iodida. Pada proses tersebut, ion timah(II) dioksidasi menjadi ion
timah(IV).
Ion timah(II) juga mereduksi ion
besi(III) menjadi ion besi(II). Sebagai contoh larutan timah(II) klorida akan
mereduksi larutan besi(III) klorida menjadi larutan besi(II) klorida. Pada
proses ini, ion timah(II) dioksidasi menjadi ion timah(IV) yang lebih stabil.
Ion timah(II) juga, tentu saja,
mudah dioksidasi oleh agen pengoksidasi yang sangat kuat seperti larutan kalium
mangan(VII) (larutan kalium permanganat) dalam kondisi asam. Reaksi ini dapat
digunakan dalam titrasi untuk menentukan konsentrasi ion timah(II) dalam suatu
larutan.
Dalam kimia organik, timah dan
asam klorida pekat digunakan untuk mereduksi nitrobenzena menjadi fenilamin
(anilin). Reaksi ini melibatkan timah yang teroksidasi menjadi ion timah(II)
dan kemudian menjadi ion timah(IV).
c.Mineral Timah
Mineral yang terkandung di dalam
bijih timah pada umumnya mineral utama yaitu kasiterit, sedangkan pirit,
kuarsa, zircon, ilmenit, plumbum, bismut, arsenik, stibnite, kalkopirit,
kuprit, xenotim, dan monasit merupakan mineral ikutan.
D.Proses Pembuatan Timah
a. proses peleburan
untuk memisahkan timah dari
pengotor-pengotornya mak biji timah harus dilebur dan di tambahkan
senyawa-senyawa lain seperti antrasite dan limestone.peleburan dilakukan di
dalam burning chamber (tanur) hingga suhu 1350°C selama 8-12jam sehingga dapat
memisahkan timah dengan pengotor-pengotornya seperti: Pb,As,Sb,Cu,Fe,Ni. Proses
peleburan imah menggunakan reduktor gas CO, gas ini dipearoleh dari pembakaran C (karbon) dalm antrasit
dengan reaksi sebagai berikut:
C(s) + O2 (g) ===> CO2(g)
CO2(g) + C(s) ===> (g)
Pada
temperatur operasi 1400°C gas CO lebih stabil dari pada gas CO2 ,
sehingga reaksi berjalan ke kanan dan diperoleh gas CO
Reaksi reduksi biji timah menjadi bebas ,
sebagai berikut :
SnO2(s)
+ CO(g) ===> SnO(s) + CO2(g)
SnO(s) + CO(g) ===> Sn(I) + CO2(g)
b.Tapping
adalah proses mengeluarkan timah
cair dan slag dalam tanur , setelah dilakukan tapping maka akan dipisahkan
antara slag dan logam timah cair , sehingga logam timah cair yang dipisahkan
dapat dicetak
c.pencetakan
proses pencetakan dilakukan
setelah mengeluarkan logam timah cair dari dalam tanur , pencetakan dilakukan
dengan menggunakan cetakan yang sudah ada . produk akhir disebut ingot
d.pemurnian
metode pemurnian menggunakan
temperatur tertentu untuk mendapatkan produk yang memilki pengotor seminimal
mungkin.
e.kegunaan timah
Banyak sekali Kegunaan Timah dan
manfaat timah terutama untuk solder, cendera mata, dan banyak digunakan pelapis
untuk melindungi logam lain dari korosi .
3.Karbon
a.sifat fisis
Simbol : C
Radius Atom : 0.91
Å
Volume Atom : 5.3
cm3/mol
Massa Atom : 12.011
Titik Didih : 5100 K
Radius Kovalensi : 0.77 Å
Struktur Kristal : Heksagonal
Massa Jenis : 2.26 g/cm3
Konduktivitas Listrik : 0.07
x 106 ohm-1cm-1
Elektronegativitas : 2.55
Konfigurasi Elektron : [He]2s2p2
Formasi Entalpi
: kJ/mol
Konduktivitas Panas : 80
Wm-1K-1
Potensial Ionisasi : 11.26 V
Titik Lebur
: 3825 K
Bilangan Oksidasi : -4,+4,2
Kapasitas Panas : 0.709
Jg-1K-1
Entalpi Penguapan : -715
kJ/mol
b.Sifat Kimia
1) Karbon bereaksi langsung
dengan fluor, dengan reaksi seperti berikut.
2) Karbon dibakar dalam udara
yang terbatas jumlahnya menghasilkan karbon monoksida.
Jika dibakar dalam kelebihan
udara, akan terbentuk karbon dioksida.
3) Membentuk asam oksi.
Bila karbon dipanaskan dalam
udara, unsur ini bereaksi dengan oksigen membentuk CO2 dan jika CO2 ini
bereaksi dengan air akan membentuk asam karbonat.
4) Membentuk garam asam oksi.
Asam karbonat, suatu asam
diprotik yang khas, bereaksi dengan basa menghasilkan karbonat dan bikarbonat,
antara lain seperti berikut.
- K2CO3 = kalium karbonat
- KHCO3 = kalium bikarbonat
- MgCO3 = magnesium karbonat
- Mg(HCO3)2 = magnesium
bikarbonat
5) Kecenderungan atom karbon
membentuk ikatan kovalen tunggal, ikatan rangkap dua dan ikatan rangkap tiga
yang akan membentuk senyawa organik.
Karbon juga merupakan bahan batu
besar dalam bentuk karbonat unsur-unsur berikut: kalsium, magnesium, dan besi.
Batubara, minyak dan gas bumi adalah hidrokarbon. Karbon sangat unik karena
dapat membentuk banyak senyawa dengan hidrogen, oksigen, nitrogen dan
unsur-unsur lainnya. Dalam banyak senyawa ini atom karbon sering terikat dengan
atom karbon lainnya. Ada sekitar sepuluh juta senyawa karbon, ribuan di
antaranya sangat vital bagi kehidupan. Tanpa karbon, basis kehidupan menjadi
mustahil.
c.Pembuatan karbon
Dalam proses pembuatan karbon
aktif berbahan dasar kulit singkong lebih baik menggunakan cara aktifasi kimia.
Diberikan proses reaksi/pembuatan ... (karbon). Kriolit berfungsi menurunkan
titik leleh Al2O3 dari 2000°C.
hidrogenasi karbon monoksida, reaksi karbonilasi, hidrogenasi senyawa tak jenuh.
dipengaruhi oleh komposisi kimia, teknik/proses pembuatan serta. Seperti pada baja karbon rendah + unsur-unsur pemadu kurang dari 4 %.
Karbon monoksida (CO) timbul karena adanya proses pembakaran yang tidak sempurna telah terjadi akumulasi beberapa unsur kimia, sehingga akan sangat berbahaya sekali. Pembuatan ruangan tempat penampung limbah padat (slag).
hidrogenasi karbon monoksida, reaksi karbonilasi, hidrogenasi senyawa tak jenuh.
dipengaruhi oleh komposisi kimia, teknik/proses pembuatan serta. Seperti pada baja karbon rendah + unsur-unsur pemadu kurang dari 4 %.
Karbon monoksida (CO) timbul karena adanya proses pembakaran yang tidak sempurna telah terjadi akumulasi beberapa unsur kimia, sehingga akan sangat berbahaya sekali. Pembuatan ruangan tempat penampung limbah padat (slag).
d.mineral karbon
Terdapat dalam mineral karbonat
yakni
batu kapur dan dolomit
batu kapur dan dolomit
e.Kegunaan Karbon
a.Bahan pembersih udara di
ruangan kandungan uap air dan gas berbau/beracun tinggi
b.Digunakan di industri obat dan
makanan sebagai penyaring, penghilang warna, bau dan rasa tidak enak pada
makanan
c.Untuk pemurnian gas.
4.Silikon
a.Sifat Fisis
Silikon berbentuk padat pada suhu
ruangan, dengan titik lebur dan titik didih masing-masing 1.400 dan 2.800
derajat celsius.Silikon mempunyai massa jenis yang lebih besar ketika dalam
bentuk cair dibanding dalam bentuk padatannya. Tapi seperti kebanyakan
substansi lainnya, silikon tidak akan bercampur ketika dalam fase padatnya,
tapi hanya meluas, sama seperti es yang memiliki massa jenis lebih kecil
daripada air. Karena mempunyai konduktivitas thermal yang tinggi (149
W·m−1·K−1), silikon bersifat mengalirkan panas sehingga tidak pernah dipakai
untuk menginsulasi benda panas.
b.Sifat Kimia
1) Silikon bereaksi dengan
halogen, secara umum reaksi yang
terjadi dapat dituliskan seperti berikut.
2) Bila silikon dipanaskan dengan
oksigen akan membentuk oksida SiO3, sehingga apabila oksida ini bereaksi dengan
air membentuk dua asam yaitu asam ortosilikat (H4SiO4) dan asam metasilikat
H2SiO3. Senyawa ini tidak larut dalam air tetapi bereaksi dengan basa.
3) Silikon membentuk garam dari
asam oksi, antara lain seperti berikut.
- Na2SiO3 = natrium metasilikat
- Mg2 SiO4 = magnesium
ortosilikat
- LiAl(SiO3)2 = litium aluminium
metasilikat
4) Semua silikat membentuk
larutan yang bersifat basa yang dapat dilarutkan dalam air, di mana ion SiO3 2¯
bertindak sebagai basa dengan menghilangkan proton dari air.
5) Silikon membentuk
molekul-molekul dan ion-ion raksasa, di mana atom oksigen menempati kedudukan
yang berselang-seling.
c.Mineral Silikon
Unsur
Na (Natrium)
Unsur
Mg (Magnesium)
Unsur
Al (Aluminium)
Unsur
Si (Silikon)
Unsur
P (Fosfor)
Unsur
Cl (Klorida)
Unsur
Ar (Argon)
D.Pembuatan Silikon
1.Dalam
Laboratorium
a.Silika
dipanaskan dalam suatu krus dengan serbuk magnesium :
Reaksi
Reduksi
SiO2(s)
+ 2 Mg(s) Si(s) + 2MgO(s)
Produk
diberikan asma klorida encer untuk menghilangkan magnesium oksida , magnesium
sisa dan magnesium silikida . kemudian , disaring yang meninggallkan serbuk
warna cukelat yang merupakan 97% silicon dan sisanya adalah silica .
b.silika
dipanaskan dengan serbuk aluminium atau seng
proses
reduksi terjadi dan silicon yang dihasillkan larut dalam leburan logam , lalu
terendapkan sebagai Kristal pada pendinginan . logam sisa kemudian dapat
dihilangkan dengan asam klorida encer , dengan menyisakan silicon yang tidak
larut
c.natrium
atau kalium dipanaskan dalam atmosfer silicon tetrafluorida . pproses reduksi
akan terjadi :
SiF4(s) + 4Na(s) ===> Si(s) + 4NaF(s)
2.Dalam Industri
Dalam industry silicon dibuat melalui pemanasan karbon
(coke) dan pasir berlebihan dalam tanur listrik sampai suhu tinggi:
SiO2(s)
+ 2C(s) Si(s) + 2CO(g)
Proses
ini dilakukan bila daya hidroelektrik dapat disesdiakan.
E.Kegunaan Silikon
a.Untuk
membuat transistor , kalkulator , komputer , dengan baterai energi matahari.
b.Untuk
operasi plastik.
c.Sebagai
lempung yang mengandung partikel silikat digunakan untuk membuat porselin tipis
berkualitas tinggi , semen portland.
d.Sebagai
silikat yang dapat digunakan untuk membuat gelas kaca.